La unidad funcional del sistema nervioso es la neurona
. Está definición fue escrita por Waldeger en 1891.
Las neuronas son células excitables del sistema nervioso, que conducen impulsos, provienen de los neuroblastos que tienen su origen en el tubo neural y en la cresta neural.
El complejo sistema nervioso de los vertebrados, en especial de los humanos, está conformado por redes perfectamente coordinadas compuestas por dichas unidades fundamentales. Por consiguiente,n o es raro entender gran diferencia en la forma y función de las diversas neuronas. En vista de esto, las neuronas se clasifican según diferentes criterios.
1.-su morfología o apariencia
2.-publicación anatómica.
3.-según sean sensitivas o motores.
4.-su velocidad de conducción.
5.-diámetro de sus fibras.
6.-si son fibras mielinizadas o no.

CLASIFICACIÓN MORFOLÓGICA.
Las neuronas son células individuales compuestas de un pericarion o cuerpo celular(suma) y un número variable de neuritas (prolongación)que se proyectan hacia el exterior, las neuronas adultas se clasifican como monopolares,bipolares,o multipolares, dependiendo de si el pericarion tiene una, dos o muchas neuritas.
CLASIFICACIÓN DE LAS FIBRAS NERVIOSAS POR GRUPOS Y CLASES.
Una neurona es aferente a un lugar en particular si conduce impulsos hacia ese lugar y es eferente de ese lugar si conduce los impulsos hacia otro sitio, por ejemplo, una neurona que transmite impulsos del tálamo a la corteza cerebral y eferente del tálamo y aferente a la corteza cerebral.
Una neurona eferente que provee de mielizacion a un musculo o a una glándula en forma directa y logra que estos reaccionen en alguna forma, se denomina. “Neurona motora”. Una neurona aferente que responde a los cambios que se presentan en el medio externo o interno, y que da origen a sensaciones conscientes se denomina “neurona sensorial”.
NERVIOS Y HACES DE LAS FIBRAS NERVIOSAS.
Las prolongaciones largas que se proyectan del suma de la celula nerviosa también se llaman fibras nerviosa.están distribuidas a lo largo de todo el sistema nervioso periférico en estructuras anatómicas independientes denominadas nervios.los nervios únicamente existen en el sistema nervisoso periférico, las fibras nerviosas se encuentran distribuidas a lo largo de todo el sistema nervioso central en agrupaciones anatómicamente separadas denominadas haces o fascículos de fibras nerviosas.
CÉLULAS DE SCHWANN
Son células no excitables del SNP que conducen impulsos.se debe recordar que estas células derivan de las células precursoras de las células de schwann de las crestas neurales primitivas. Y se desarrollan al mismo tiempo que todos los neuroblastos del sistema nervioso periférico. Las células de Schwann envuelven frecuentemente el axón de una neurona en desarrollo, de manera que colocan capa sobre capa de mielina hasta producir una neurona mielinizada.en otras ocasiones el desarrollo no se caracteriza por la presencia de capas de mielina originada por las células de schwann, por consiguiente esta neurona permanece desmielinizada.
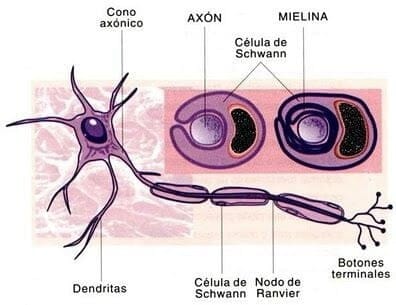
NEURONAS MIELINIZADAS
En neuronas destinadas a contar con vaina de mielina en su estructura, una célula de schwann comienza a enrollarse en forma espiral alrededor de cierta longitud del axón. Al llevar a cabo este proceso, La célula de schwann expulsa su citoplasma a medida que sus dos membranas se aproximan entre sí, en esta forma, la célula coloca capa sobre capa de su propia membrana. Hasta formar una vaina laminada de un material que contiene gran cantidad de fosfolípidos denominada mielina.
NEURONAS NO MIELINIZADAS
Las fibras autónomas postganglionares, lo mismo que algunas fibras nerviosas delgadas que provienen de receptores del dolor y la temperatura, guardan poca relación con las células de schwann una de estas clase de fibras nerviosas que generalmente se encuentran en unas depresiones o surcos profundos y largos de las células de schwann. Una de estas células puede alojar parcialmente varias fibras angostas. En este caso, la diferencia de lo que ocurre en los axones mielinizados,el líquido extracelular del tronco nervios esta en conducta con la membrana axónica a través de un orificio en el mesaxon que está en comunicación con el espacio periaxonico,por tanto, todo el axón no mielínico está en comunicación con el espacio periaxonico.por tanto, todo el axón no mielínico está en contacto permanente con un espacio en el cual se puede llevar a cabo un intercambio libre de líquidos por consiguiente. El patrón de conducción de impulsos no es saltatorio con lo es en los axones mielinizados, aunque las células de schwann están en contacto permanente con estos axones, esta no están mielanizadas, debido a que las envuelven las células.


CELULAS DE LA NEUROGLIA
La neuroglia (pegamento neural) es una fina red de tejido, compuesta de células neurogliales.se encuentran únicamente en el sistema nervioso central y se dividen en 2 categorías, macroglia y microglia.
Las células macrogliales se originan a partid de glioblastos del tubo neural e incluyen unas células pequeñas en forma de estrellas denominados astrocitos, lo mismo que los oligodendrocitos, que son en el SNC el equivalente de las células de schwann los microgliocitos son células pequeñas no neurales. Posiblemente de origen mesodérmico.
Las células neurogliales.desempeñan múltiples funciones en el SNC.
Los astrocitos parecen intervenir en el transporte de materiales a las neuronas del sistema nervioso central, lo mismo que influyen sobre las funciones necesarias para mantener un medio iónico apropiado para las neuronas.
Los oligodendrocitos son responsables de la mielinizacion de las neuronas del sistema nervioso central. Sin embargo en contraste con una célula de schwann que solo puede mielinizar un solo axón, cada oligodendrocito puede mielinizar un solo axón, cada oligodendrocito puede mielinizar axones de varias neuronas del SNC.como se mencionó con anterioridad, es muy probable que los microgliocitos no tengan su origen en SNC.son células pequeñas de formas diversas con finas prolongaciones ramificadas que se desplazan hacia el SNC actuando como fagocitos que engloban los productos de desecho y de descomposición de las neuronas del SNC.
CÉLULAS EPENDIMARIAS.
Es importante recordar que el epéndimo es una capa sencilla de células epiteliales que recubre los ventrículos del cerebro y el conducto central de la médula espinal tienen su origen en las células neuroepiteliales fijas que revisten en su interior al tubo neural posteriormente se diferencien y transforman en la cobertura ependimaria del sistema nervioso central.
POTENCIAL DE MEMBRANA O POTENCIAL DE ACCIÓN
La membrana está formada por una bicapa lipídica, por proteínas periféricas en la parte interna y externa y por proteínas integrales que atraviesan de punta a punta la membrana, son las llamadas canales por donde pasan los iones. Estos canales pueden estar en estados diferentes y abiertos o cerrados.
Se ha medido la composición que tiene el líquido extracelular e intracelular y se ha averiguado que es diferente.
CONCENTRACIONES PARA DIFERENTES IONES.
Se describe la llamada teoría de Singer y Nicolson (1972) o teoría del mosaico fluido.
La membrana está formada por una bicapa lipídica, por proteínas periféricas en la parte interna y externa y por proteínas integrales que atraviesan de punta a punta, la membrana, son los llamados canales por donde pasan los iones.
Estos canales pueden estar en estados diferentes, abiertos o cerrados.

Cuando una célula está en reposo (no estimulada ni excitada) los canales de potasio están abiertos, él potasio tendera a salir hacia el exterior (iones de k) son cargas positivas por tanto el interior celular será negativo respecto al exterior celular.
POTENCIAL DE REPOSO BASE IÓNICAS
Todas las c células tienen potencial de reposo (hepatocito) en base a una diferencia iónica dentro y fuera de la célula, pero no todas tienen capacidad de desarrollar potenciales de acción.
células tienen potencial de reposo (hepatocito) en base a una diferencia iónica dentro y fuera de la célula, pero no todas tienen capacidad de desarrollar potenciales de acción.
Las células excitables (neuronas) poseen un potencial de reposo muy estable (entre -60 y 100 mv)
En las células no excitables, él potencial de reposo es menos estable, pueden haber oscilaciones entre (-40 y -60 mv), está más despolarizado.}También se puede medir mediante la ecuación de Goldman.
Ecuación de Nernst. Ecuación de Goldman reducida a un solo ion.
R=constante general de los gases
T=temperatura es grados kelum
Z=valencia.
F=constate de farada
E=poder de equilibrio.}
(Calculado el potencial de Nernst es más aproximado el reposo de esa célula)
El potencial de reposo se debe principalmente a la permeabilidad a otros iones.
La contracción sincronizada de todas las células que están copladas eléctricamente constituyendo el tejido cardiaco, genera la contracción sincrónica de cada una de las cámaras del corazón.
La contracción de cada célula está asociada a un potencial de acción.
POTENCIAL DE MEMBRANA O POTENCIAL DE ACCIÓN
1.- POTENCIALES DE MEMBRANA
Normalmente hay potenciales eléctricos a través de las membranas en todas las células. De las cuales:
· Las células nerviosas y musculares son AUTOEXCITABLES
· Es decir, son capaces de autogenerar impulsos electroquímicos
· En sus membranas, y en muchos casos, de transmitir señales a
· Lo largo de las mismas.
1.1.-POTENCIALES DE MEMBRANA CREADAS POR DIFUSIÓN
[ Na +] intracelular > [ Na ] intracelular = difunde = > cargas + intracel = pero, luego la difusión se frena por esas cargas (+) = POTENCIAL DE NERNST

1.2.-CONCEPTOS
Cuando el potencial de membrana es generado por la por difusión de diferentes iones (por diferente permeabilidad a la membrana)
Depende de:
* Polaridad de la carga eléctrica de cada ion.
* Permeabilidad de la membrana para cada ion.
* [ ] De cada uno de los iones en el int-ext celular.
Esos iones son:
Na+ K+ Cl-
= desarrollan potenciales de membrana en membranas de células neuronales, musculares y nervios de conducción.
= el gradiente de [ ] de cada uno a través de la membrana determina el VOLTAJE del potencial de membrana
La permeabilidad de los canales de Na y K sufren cambios durante la conducción del impulso nervioso. Mientras que los canales de Cl. no cambian, por lo tanto los cambios de
Permeabilidad para Na y K son importantes para la: TRANSMISIÓN DE LA SEÑAL A LOS NERVIOS.
Potencial de reposo en la membrana de la célula nerviosa
· De reposo: cuando no están transmitiendo señales = - 90 Mv
· Es producido por:
· DIFUSIÓN PASIVA DEL K: a través de un canal proteico = - 94 Mv
· DIFUSIÓN PASIVA DEL Na: a través de canales proteicos pero con menos permeabilidad que el K = + 61 Mv
La combinación de ambos genera un POTENCIAL NETO de – 86 Mv. Donde la bomba de sodio y potasio es:
BOMBA Na-K: Saca 3 Na+ y mete 2 K = - 90 Mv
2.-El potencial de acción
· Permite transmitir señales nerviosas en las células nerviosas que Son cambios rápidos del potencial de membrana = y que se desplaza a lo largo de la fibra nerviosa.
· ETAPAS:
· REPOSO: la membrana está POLARIZADA con – 90 MV
· DESPOLARIZACIÓN: > permeab Na - entra Na a la cel. - se positiviza el interior de la célula (porque el potencial de membrana disminuye a -50-70 Mv y se abren canales de Na por VOLTAJE)
· REPOLARIZACIÓN: < permeab K = sale K al ext. = se negatividad el interior celular nuevamente.
2.1.-Inicio del potencial de acción
· Cualquier acontecimiento que aumente RÁPIDAMENTE el potencial
· De membrana y sobrepase el UMBRAL alrededor de los – 65 Mv
· Provocará que se abran los canales de Na (por voltaje) en forma PROGRESIVA y RECLUTANTE.
2.2.-Propagación del potencial de acción
Es decir, un potencial de acción de un SEGMENTO EXCITABLE de la membrana puede excitar segmentos adyacentes = la PROPAGACIÓN DE LA DESPOLARIZACIÓN a lo largo de:
* La fibra nerviosa = impulso nervioso = POT ACC (>1 para que la fibra muscular = impulso muscular = UMBRAL se de la propagación) como un "FACTOR DE SEGURIDAD"
2.3.-Potencial de acción en meseta
· A: DESPOLARIZACIÓN. por canales rápidos de Na abiertos por volt.
· B: MESETA. Prolongación del Tiempo de despolarización = T de contracción muscular cardiaca. Es por canales lentos de Ca por voltaje
· C: REPOLARIZACIÓN. Por entrada de K (abertura de canales de K) y termina entrada de Na (se cierran los canales)
3.-La ritmicidad de ciertos tejidos excitables
En base a la alta permeabilidad a los Na (y Tb. CA) para permitir la DESPOLARIZACIÓN AUTOMÁTICA.
El potencial de membrana en reposo es de – 60 a – 70 Mv
Estas descargas repetitivas se dan en neuronas, músculo liso y cardiaco. En donde se manifiestan como ritmo cardiaco, perístasis y ritmo respiratorio. Tb hay una HIPERPOLARIZACIÓN al final del potencial de acción, debido a canales de K = una excesiva permeabilidad al K y eso retrasa. La siguiente despolarización.
4.-El fenómeno de excitación
Cualquier fenómeno que aumente la permea bilidad al Na producirá la apertura de los canales de Na automáticamente.
bilidad al Na producirá la apertura de los canales de Na automáticamente.
Pueden ser:
· fenómenos físicos
· fenómenos químicos
· fenómenos eléctricos
y Los ESTABILIZADORES DE LA MEMBRANA Inhiben la excitabilidad (hipercalcemia, hipocalcemia, procaína, Tetracína, por disminución de activación de canales de Na)
A. Aquí se describe la llamada Teoría de Singer y Nicolson (1972) o Teoría del mosaico fluido.
La membrana está formada por una bicapa lipídica, por proteínas periféricas en la parte interna y externa y por proteínas integrales que atraviesan de punta a punta la membrana, son los llamados canales por donde pasan los iones. Esos canales pueden estar en estados diferentes, abiertos o cerrados.
Se ha medido la composición que tiene el líquido extracelular e intracelular y se ha averiguado que es diferente.
B. CONCEPTO DE POTENCIAL DE MEMBRANA O DE ACCIÓN
C. BASES IÓNICAS DEL POTENCIAL DE REPOSO
CONCENTRACIONES PARA DIFERENTES IONES
IONES | INTRACELULAR | EXTRACELULAR |
Na + | 14 mM | 142 mM |
K - | 140 mM | 4 mM |
Cl - | 4 mM | 120 mM |
HCO 3 - (bicarbonato) | 10 mM | 25 mM |
H + (hidrogeniones) | 100 mM | 40 mM |
Mg 2 + | 30 mM | 15 mM |
Ca 2 + | 1 mM | 18 mM |
Mg 2 + | 30 mM | 15 mM |
Ca 2 + | 1 mM | 18 mM |
Cuando una célula está en reposo (no estimulada ni excitada) los canales de potasio están abiertos, el potasio tenderá a salir hacia el exterior (iones de K), son cargas positivas por tanto el interior celular será negativo respecto al exterior celular
POTENCIAL DE REPOSO. BASES IÓNICAS

Todas las células tienen potencial de reposo (hepatocito) en base a una diferencia iónica dentro y fuera de la célula, pero no todas tienen capacidad de desarrollar potenciales de acción.
Las células excitables (neuronas) poseen u potencial de reposo muy estable (entre -60 y -100 mV). En las células no excitables, el potencial de reposo es menos estable, pueden haber oscilaciones entre (-40 y -60 mV), está más despolarizado.
También se puede medir mediante la Ecuación de Goldman
Ecuación de Nernst. Ecuación de Goldman reducida a un solo ión.
R = Constante general de los gases
T = Temperatura es grados kelvin
Z = valencia
F = constante de FaradaE = poder de equilibrio (calculado el potencial de Nerst es más aproximado el reposo de esa célula).
El potencial de reposo se debe principalmente a la permeabilidad a otros iones.
La contracción sincronizada de todas las células que están acopladas eléctricamente constituyendo el tejido cardíaco, genera la contracción sincrónica de cada una de las cámaras del corazón.
La contracción de cada célula está asociada a un potencial de acción.
Hay que tener en cuenta:
· El potencial de reposo siempre es negativo. – 80 mv.· Colocar un electrodo en el interior de la célula y otro en el exterior
· El interior celular siempre es negativo
· La permeabilidad más importante durante el potencial de reposo en la de potasio
· También participan pero con muchísima menor permeabilidad otros iones como el sodio,
· También participan la bomba sodio potásica electrogénica, intercambia iones,

3 moléculas de Na, por 2 moléculas de K, por cada molécula de ATP hidrolizada. De esta manera ese poquito sodio que se había perdido es devuelto al interior de la célula.
A. CONCEPTO DE POTENCIAL DE ACCIÓN BASES IÓNICAS
Todas las células poseen potencial de reposo pero no todas son capaces de generar un potencial de acción. Las células excitables que generan potenciales de acción son:
· Neuronas. Células nerviosas
· Células musculares. Músculo liso (vísceras internas, útero, uréteres e intestino), músculo estriado (músculo esquelético y del corazón)
· Células sensoriales. Preceptores de la vista y del oído
· Células secretoras. Glándulas salivares, parótida
· Células relacionadas con el sistema Endocrino. Adenohipófisis, islote de Langerhans (insulina)
El hepatocito no requiere un potencial de acción. Las células las podemos estimular de forma:
· Mecánica. Punzón
· Química. Con un neurotransmisor
· Eléctrica. Es la más parecida a la fisiología y mide exactamente la intensidad del estímulo que estamos aplicando a esa célula.
El potencial de acción de la fibra nerviosa dura de alrededor de unos 2 msg, en la fibra muscular esquelética también son excitables, es similar al potencial reacción pero tienen mayor amplitud 5 msg.
El potencial de acción en la fibra muscular cardiaca tiene características distintas, posee una gran meseta y su amplitud es mucho mayor 200 msg.
El potencial de acción se caracteriza porque existe una inversión de la polaridad, el interior celular negativo pasa a positivo en el momento en que el potencial de acción pasa por ahí. El potencial de acción no es decremencial, no disminuye durante su traslado, es mantenido.
A. PROPAGACIÓN DEL POTENCIAL DE ACCIÓN:
LEY DEL TODO O NADA
El potencial de acción responde a la ley de todo o nada, el potencial para que tenga lugar necesita de un estímulo liminal que llegue al punto crítico de dispara de esa célula.
a. Despolarización lenta. -70 mv hasta -55 mv
b. Despolarización rápida. - 55 mV hasta +35 mV.
c. Repolarización rápida. + 35 mv 2/3 del descenso
d. Repolarización lenta (hasta - 70 mV)
e. Hiperpolarización. -70 mV hasta - 75 mV.
El potencial de acción se produce o no siendo igual. No se produce si el estímulo no alcanza el punto crítico de la célula, y si se supera si que hay potencial. La ley se cumple para fibras aisladas, para una fibra única, pero no se cumple cuando existen múltiples fibras nerviosas (axones)
E. BASES IÓNICAS
En 1954, dos investigadores llamados Hodgkin y Huxley midieron las corrientes iónicas que suceden durante el potencial de acción.
Las bases iónicas son:
· Permeabilidad al sodio y al potasio
· Despolarización al sodio y al potasio
· Repolarización al sodio y al potasio
Se observan cambios de conductancia para el Na y el K durante el potencial de acción. Durante la despolarización y repolarización midieron la conductancia.
El potencial de acción en su fase de despolarización existe un aumento de la permeabilidad del Na (hay más Na fuera por eso entra), es básicamente en la neurona, fibra muscular. En el caso de la producción de insulina aumentará la permeabilidad del calcio.
La repolarización es debida a un aumento del pk, siempre debido a la conductancia al K (salida del K). Además pueden aparecer otros iones que estudian morfologías un poco distintas.
El potencial de equilibrio para el sodio se puede calcular utilizando la ecuación de Golman, para la medida exacta lo mejor es el registro intracelular.
La bomba sodiopotásica electrogénica también participa porque tiene la capacidad de devolver a su sitio los iones
A. CONDUCCIÓN DEL IMPULSO NERVIOSO O ASPECTOS ESPECILAES DE TRAMSMISIÓN DE SEÑALES EN LOS TRONCOS NERVIOSOS.
· PERÍODOS REFRACTARIOS
Supone una situación de inestabilidad de la membrana cuando una célula acaba de ser estimulada y acaba de generar un potencial de acción, el potencial de acción inmediatamente no puede generar otro.
· Absoluto: período de tiempo inmediatamente después de un potencial de acción en donde no hay respuesta independientemente de la intensidad del estímulo que se le aplique.
· Relativo: período de tiempo después del período absoluto en donde si que hay respuesta pero sólo si se le aplica una intensidad de estímulo por encima del umbral de excitación de la célula
· TEORÍA DE LOS CIRCUITOS LOCALES O TEORIA DEL POZO O FUENTE
Por el hecho de existir cargas positivas al lado de negativas se generan unas corrientes locales que van desde el positivo al negativo, esa corriente va a ser la que va a ir desplazando la zona vecina. No se puede volver hacia atrás porque está el período refractario absoluto.
Existen dos tipos de células nerviosas:
· Neuronas mielínicas
· Neuronas no mielínicas.
La conducción del impulso nervioso es diferente para cada una de ellas. La conducción nerviosa en las fibras mielínicas es una transmisión rápida, por término medio tienen unas 20 cm de diámetro con una velocidad de conducción de unos 100 m/sg.
El potencial de acción es enviado mediante la Teoría saltatoria, lo que hace esa despolarización es que va saltando de nodo de Ranvier en nodo.
La transmisión sin mielina es lenta por término medio de 0,5 um de diámetro y la velocidad de conducción de alrededor de 0,5 m/sg, la transmisión se va produciendo en toda la zona de axón.
La transmisión del impulso nervioso saltatorio de las células con melina es más económica energéticamente para el organismo. Una molécula de ATP intercambia 3 de Na y 2 de K.
La velocidad de conducción se mide conociendo 2 parámetros.
· La distancia entre el estimulador y el registrador
Potencia (tiempo transcurrido entre en encendido de Ohm y el inicio del potencial de acción).
El potencial de acción se caracteriza porque existe una inversión de la polaridad, el interior celular negativo pasa a positivo en el momento en que el potencial de acción pasa por ahí. El potencial de acción no es decremencial, no disminuye durante su traslado, es mantenido.
A. PROPAGACIÓN DEL POTENCIAL DE ACCIÓN:
LEY DEL TODO O NADA
El potencial de acción responde a la ley de todo o nada, el potencial para que tenga lugar necesita de un estímulo liminal que llegue al punto crítico de dispara de esa célula.
a. Despolarización lenta. -70 mv hasta -55 mv
b. Despolarización rápida. - 55 mV hasta +35 mV.
c. Repolarización rápida. + 35 mv 2/3 del descenso
d. Repolarización lenta (hasta - 70 mV)
e. Hiperpolarización. -70 mV hasta - 75 mV.
El potencial de acción se produce o no siendo igual. No se produce si el estímulo no alcanza el punto crítico de la célula, y si se supera si que hay potencial. La ley se cumple para fibras aisladas, para una fibra única, pero no se cumple cuando existen múltiples fibras nerviosas (axones)
E. BASES IÓNICAS
En 1954, dos investigadores llamados Hodgkin y Huxley midieron las corrientes iónicas que suceden durante el potencial de acción.
Las bases iónicas son:
· Permeabilidad al sodio y al potasio
· Despolarización al sodio y al potasio
· Repolarización al sodio y al potasio
Se observan cambios de conductancia para el Na y el K durante el potencial de acción. Durante la despolarización y repolarización midieron la conductancia.
El potencial de acción en su fase de despolarización existe un aumento de la permeabilidad del Na (hay más Na fuera por eso entra), es básicamente en la neurona, fibra muscular. En el caso de la producción de insulina aumentará la permeabilidad del calcio.
La repolarización es debida a un aumento del pk, siempre debido a la conductancia al K (salida del K). Además pueden aparecer otros iones que estudian morfologías un poco distintas.
El potencial de equilibrio para el sodio se puede calcular utilizando la ecuación de Golman, para la medida exacta lo mejor es el registro intracelular.
La bomba sodiopotásica electrogénica también participa porque tiene la capacidad de devolver a su sitio los iones
A. CONDUCCIÓN DEL IMPULSO NERVIOSO O ASPECTOS ESPECILAES DE TRAMSMISIÓN DE SEÑALES EN LOS TRONCOS NERVIOSOS.
· PERÍODOS REFRACTARIOS
Supone una situación de inestabilidad de la membrana cuando una célula acaba de ser estimulada y acaba de generar un potencial de acción, el potencial de acción inmediatamente no puede generar otro.
· Absoluto: período de tiempo inmediatamente después de un potencial de acción en donde no hay respuesta independientemente de la intensidad del estímulo que se le aplique.
· Relativo: período de tiempo después del período absoluto en donde si que hay respuesta pero sólo si se le aplica una intensidad de estímulo por encima del umbral de excitación de la célula
· TEORÍA DE LOS CIRCUITOS LOCALES O TEORIA DEL POZO O FUENTE
Por el hecho de existir cargas positivas al lado de negativas se generan unas corrientes locales que van desde el positivo al negativo, esa corriente va a ser la que va a ir desplazando la zona vecina. No se puede volver hacia atrás porque está el período refractario absoluto.
Existen dos tipos de células nerviosas:
· Neuronas mielínicas
· Neuronas no mielínicas.
La conducción del impulso nervioso es diferente para cada una de ellas. La conducción nerviosa en las fibras mielínicas es una transmisión rápida, por término medio tienen unas 20 cm de diámetro con una velocidad de conducción de unos 100 m/sg.
El potencial de acción es enviado mediante la Teoría saltatoria, lo que hace esa despolarización es que va saltando de nodo de Ranvier en nodo.
La transmisión sin mielina es lenta por término medio de 0,5 um de diámetro y la velocidad de conducción de alrededor de 0,5 m/sg, la transmisión se va produciendo en toda la zona de axón.
La transmisión del impulso nervioso saltatorio de las células con melina es más económica energéticamente para el organismo. Una molécula de ATP intercambia 3 de Na y 2 de K.
La velocidad de conducción se mide conociendo 2 parámetros.
· La distancia entre el estimulador y el registrador
Potencia (tiempo transcurrido entre en encendido de Ohm y el inicio del potencial de acción).
Factores que condicionan la velocidad de conducción
· El diámetro de la fibra. A mayor diámetro, mayor velocidad de conducción. Existe una relación entre el incremento del diámetro y en incremento de la velocidad de conducción.
La temperatura. La velocidad de conducción se eleva progresivamente al elevar la temperatura, desde 5ºC hasta 40ºC, a partir de lNeurofisiología de las Sinapsis. Dr.
Roberto Rosler.
Abreviaturas:
· NT: Neurotransmisores.
· SN: Sistema Nervioso.
· SNC: Sistema Nervioso Central.
· SNP: Sistema Nervioso Periférico. CONTENIDOS
· Definición de Sinapsis.
· Clasificación.
· Características generales de Sinapsis Eléctrica.
· Características generales de Sinapsis Química.
· Síntesis del Neurotransmisor (NT).
· Almacenamiento de NT.
· Liberación de NT.
· Interacción del NT con el Receptor.
· Desactivación del NT.
Contenidos
La palabra Sinapsis viene del griego “Sinaptein” que significa “Estar juntos”
Definición de Sinapsis: Zona de contacto funcional entre dos células excitables especializadas en la transmisión de impulsos bioeléctricos.
Por lo tanto una sinapsis puede establecerse, por ejemplo, entre:
· Dos Neuronas.
· Una Neurona y una célula muscular.
· Una Neurona y una célula endocrina.

Diversos Fármacos y Enfermedades Mentales modifican el funcionamiento de las Sinapsis.
El Aprendizaje mismo es fundamentalmente un aumento de la eficacia Sináptica.
Clasificación:}
Hay diversos criterios para clasificar una Sinapsis:
Según el tipo de Neurotransmisor:
1. Aminas Biógenas: Noradrenalina, Serotonina, Acetilcolina, Dopamina, Histamina.
2. Péptidos: Endorfinas, Sustancia P, etc.
3. Aminoácidos: Glutamato, Aspartato, GABA, Glicina. Según el tipo de Transmisión:
1. Química (Rápida o Lenta).
2. Eléctrica. 3.
Mixta. Según las zonas neuronales que entran en contacto:
1. Axo-Dendrítica
2. . 2. Axo-Somática. 3
3. . Axo-Axónica. 4.
4. Dendrodendrítica.
Sinapsis Eléctrica
En este tipo de Sinapsis ambas porciones de las neuronas en contacto están muy cercanas entre sí y están unidas por espacios de interconexión
denominados Conexiones que conforman canales iónicos que intercomunican ambas células.
Las Sinapsis eléctricas:
1. · Son Bidireccionales o sea que el estímulo eléctrico puede ser transmitido desde la neurona A hacia la B y desde la neurona B a la A.
2. · La transmisión es Infalible, o sea que siempre logra generarse un Potencial de Acción en la Neurona Postsináptica.
3. · Transmiten el Potencial de Acción a gran velocidad. Son poco frecuentes: · Se observan en el Sistema Nervioso fetal donde cumplirían con la función de coordinar la maduración de diferentes grupos neuronales.
4. · En el Sistema Nervioso adulto se las encuentra relacionadas con los reflejos de Huida y en el Hipotálamo con el objetivo de sincronizar las descargas neuronales.
5. · Son el primer tipo de Sinapsis que apareció en la escala Filogenética.
Sinapsis Química:
Dos ejemplos típicos de una Sinapsis Química son las uniones entre dos neuronas y las de una neurona con una fibra muscular (Sinapsis neuromuscular).
6. Las Sinapsis Químicas se caracterizan por ser Unidireccionales o sea que las señales bioeléctricas sólo pueden transmitirse de la neurona A a la neurona B. En la Sinapsis química se lleva a cabo una doble traducción. Lo que llega al terminal axonal es una señal eléctrica (un potencial de acción) que es traducida en una señal química (liberación de neurotransmisores hacia la hendidura sináptica). La señal química (el neurotransmisor), luego de interactuar con los receptores postsinápticos, es nuevamente traducida a una señal eléctrica (los potenciales postsinápticos). Estos potenciales al arribar al cono axonal, si llegan a su valor umbral, generarán un potencial de acción que viajará hacia el terminal axonal de la neurona postsináptico para ser nuevamente “traducido
7.
Sinapsis y Desarrollo Embriológico:
Debemos aclarar que las “conversaciones” entre neuronas no se restringen a los neurotransmisores. También existen otros tipos de “conversaciones” ínter neuronales como, por ejemplo, en el desarrollo fetal. Durante este desarrollo las células nerviosas se envían información mediante:
· Moléculas de adhesión que guían la migración de las neuronas hacia su destino final[1].
· Factores tróficos (Neurotrofinas) de los cuales depende la supervivencia de las neuronas durante el desarrollo embriológico. Otro aspecto importante es que tanto durante el período fetal como en la niñez hay una eliminación sináptica de aquellas conexiones supernumerarias. Esta “poda” sináptica es realizada “sabiamente”: Entre los 6 y los 14 años hay un decremento del número de sinapsis desapareciendo las conexiones que no han sido utilizadas. Esto destaca la gran importancia del aprendizaje y la estimulación en el niño para disminuir esta pérdida por “poda” sináptico
1.- Síntesis del NT: Los Neurotransmisores se sintetizan mediante la acción de diferentes enzimas sobre sustancias “precursoras” que son captadas por las neuronas del líquido extracelular. Existe un grupo de neurotransmisores (aminas biógenas y aminoácidos) que son sintetizados directamente en la zona de liberación (terminal pre sináptico). Las enzimas necesarias para esta síntesis de los NT son “fabricadas” en el soma de la neurona (donde está su “maquinaria” síntesis). Por lo tanto, para los neurotransmisores que son sintetizados en el terminal pre sináptico, las enzimas “viajarán” desde el soma celular hasta dicho terminal mediante el transporte axonal anterógrado. Otro grupo, los NT peptídicos, son sintetizados en el soma celular ya que se trata de moléculas grandes de gran complejidad bioquímica. Una vez sintetizados estos NT serán trasladados mediante el transporte axonal anterógrado hasta el terminal pre sináptico
2.- Almacenamiento del NT: Una vez sintetizado el NT es almacenado en una vesícula (que es una especie de “bolsa membranosa”) para ser protegido de las enzimas que “nadan” en el líquido intracelular y que pueden destruirlos.
O sea que la vesícula es una especie de “empaquetadora” que “secuestra” al NT para evitar que sea “degradado 3.- Liberación del NT: La liberación del NT es una “neurosecreción” que surge como consecuencia de una despolarización del terminal pre sináptico.” por las enzimas.
Entre la señal eléctrica y la neurosecreción de NT hay un “intermediario” que actúa como mensajero intracelular que es el Calcio que aumenta a grandes concentraciones en el líquido intracelular luego de la despolarización. Como ya hemos descrito las vesículas se encuentran “ancladas” en regiones que tienen una gran cantidad de canales de calcio que se abren como consecuencia de la llegada de la despolarización y esto explica el rápido e importante incremento del Calcio intracelular. Esta es la base de la “inaudita” velocidad de la liberación del NT: ¡desde que entra el Calcio hasta que se produce la exocitosis pasan solamente 0,18 milisegundos! ¿Puede imaginarse que representa esta cifra en el contexto temporal [2]? ¿Cómo logra el Calcio que se produzca la exocitosis del contenido vesicular? Existe un grupo de proteínas en la pared de la vesícula que debe ser activada para que se genere la exocitosis. El activador es el Calcio que al unirse a estas moléculas desencadena el proceso que termina con la liberación del NT en la hendidura sináptica.
3.- Interacción del NT con el Receptor postsináptico: El NT actúa como un “puente” químico ya que es el resultado de un cambio bioeléctrico en la neurona presináptica y al unirse con el receptor “gatillar” un cambio eléctrico en la neurona postsináptica. El Receptor es una proteína que puede estar acoplada a: · Un canal iónico y entonces se lo denomina Receptor Ionotrópico[3]. · Proteínas intracelulares que actúan como segundos mensajeros y en estos casos se lo denomina Receptor Metabotrópico[4]. Si el NT se une a un receptor ionotrópico se genera un cambio de permeabilidad en la membrana postsináptica que causará una modificación bioeléctrica.
Dicho cambio bioeléctrico puede ser
: Despolarizante: Acercará el Potencial de Membrana a su valor Umbral y aumentará las posibilidades de generar un PA. Por esto se lo denomina Potencial Excitatorio Postsináptico (PEPS para los amigos). Se puede generar un PEPS, por ejemplo, aumentando la permeabilidad al Na o disminuyendo la permeabilidad al K. Hiperpolarizante: Alejará al Potencial de Membrana del Valor Umbral y disminuirá las posibilidades de generar un PA. Por esto se lo denomina Potencial Inhibitorio Postsináptico. (PIPS para los amigos). Se puede generar un PIPS, por ejemplo, aumentando la permeabilidad al Cl o disminuyendo la permeabilidad al Na. Debido a que una misma neurona puede recibir miles de aferencias, cada una de estas aferencias puede generar a través de sus conexiones sinápticas cambios bioeléctricos (PEPS o PIPS) en la neurona postsináptica. El cono axónico es el lugar de la génesis del Potencial de Acción[5], que es la respuesta bioeléctrica de la neurona postsináptica ante la estimulación de sus múltiples aferencias. Cada uno de los potenciales postsinápticos generados por las aferencias presinápticas es como un “voto” electrónico que será sumado en el cono axónico. Si esta “votación” llega al umbral de membrana del Cono se generará un Potencial de Acción. De esta manera vemos que la integración en la neurona postsináptica de la información aferente que recibe es una especie de “contienda” iónica entre los PEPS y los PIPS recibidos en las Dendritas. Estos se propagan a través del soma para llegar al cono axónico y allí se decide la “batalla” según si se llega o no al valor umbral de esta zona.
Receptores presinápticos: Nacidos para controlar. Pero además de los receptores postsinápticos existen también los receptores presinápticos unidos a la porción externa de la membrana de la neurona presináptica. Estos receptores presinápticos pueden dividirse en auto-receptores hetero-receptores presinápticos (receptores para NT que no son los liberados por la neurona presináptica sino por las neuronas vecinas). presinápticos (receptores para el tipo de NT que libera la neurona presináptica) y en la función de los auto-receptores presinápticos es la de control por retroalimentación negativa por la misma neurona que libera el NT. Esto quiere decir que cuando el NT liberado a la hendidura llega a una concentración determinada impide que la neurona presináptica siga liberando NT (Control por retroalimentación auto inhibitoria de la liberación de NT). Los hetero-receptores presinápticos posibilitan el control de la liberación de NT de la porción presináptica por parte de las neuronas vecinas. La función de los hetero-receptores presinápticos es la de control por retroalimentación negativa por las neuronas vecinas a la que libera el NT. Los NT que actúan sobre los receptores ionotrópicos (como por ejemplo muchas aminas biógenas y los aminoácidos) suelen tener una acción rápida y corta. Esto se debe a que al estar estos receptores directamente relacionados con canales iónicos (químicamente excitables ya que es el NT es que los abre o cierra) se generan cambios iónicos casi instantáneos (en menos de un milisegundo) de corta duración. Los NT peptidérgicos suelen tener una acción lenta y prolongada ya que actúan sobre receptores metabotrópicos que están acoplados a la Proteína G. La Proteína G activa a segundos mensajeros que son una especie de “correos” intracelulares que pueden generar cambios moleculares (citoplasmáticos o en los genes) que se inician lentamente pero que pueden durar mucho tiempo (horas, días o hasta meses). ¡Hay más de 100 tipos de receptores metabotrópicos!
Los receptores metabotrópicos generan PEPS y PIPS de lenta aparición y de larga duración. Estos receptores afectan a los canales indirectamente a través de moléculas transductoras como la Proteína G que acopla la unión del NT con el receptor postsináptico con la regulación de la apertura o cierre de los canales iónicos
Esta acción de la proteína G sobre un canal iónico puede seguir tres secuencias: 1. Proteína G actuando directamente sobre un canal iónico. 2. Proteína G actuando sobre un segundo mensajero que a su vez modifica la función de un canal iónico. 3. Proteína G actuando sobre un segundo mensajero que entra al núcleo celular y modifica la expresión de genes cambiando la síntesis de canales iónicos (aumentando o disminuyendo su número en la membrana postsináptica
¿Por qué existen dos tipos de transmisión química (iono y metabotrópica)? Un Sistema Nervioso que cuente únicamente con un flujo de información rápida (inotrópica) sólo es capaz de respuestas estereotipadas[6]. Los receptores metabotrópicos posibilitan mecanismos de adaptación y plasticidad modificando las respuestas y, por lo tanto,
“aprendiendo” otro tipo de resoluciones. Existen múltiples sinapsis en el SN en las cuales existe cotransmisión. Se dice que existe cotransmisión cuando en una misma sinapsis hay dos tipos de NT (uno de los cuales actúa a través de receptores ionotrópicos y el otro sobre receptores metabotrópicos). En estos tipos de Sinapsis hay diferentes tipos de NT para “expresar” diferentes estados funcionales de la neurona presináptica hacia la neurona postsináptica. Ejemplos de Neurotransmisores: Glutamato: Es el NT más frecuente en el SNC: se encuentra en más del 50% de sus sinapsis. Es un NT excitatorio (despolarizante – PEPS) y si su nivel en la hendidura se eleva por encima de sus valores normales se transforma en un NT “asesino”.
Produce la necrosis de las neuronas vecinas por excito-toxicidad. Literalmente las excita hasta su muerte. La elevación del Glutamato produce un aumento de la permeabilidad del Calcio con su consecuente aumento en el LIC. Este aumento activa diferentes proteasas citoplasmáticas que auto digieren a la neurona. La excito-toxicidad es un mecanismo muy importante de lesión celular en los Traumatismos de Cráneo y las Isquemias Cerebrovasculares. El Glutamato está también relacionado con los mecanismos de aprendizaje sináptico. GABA: Es el principal NT inhibidor (hiperpolarizante – PIPS) del SN. Un 33% de sinapsis tienen GABA como NT. Aumenta la permeabilidad al Cloro, lo que explica la hiperpolarización que genera. Las benzodiacepinas (como, por ejemplo, el Valium) actúan potenciando la acción del GABA. Por eso cuando tomamos una de estas pastillas, el “Nirvana” químico en el que entramos (donde nadie puede molestarnos) se debe a que el potencial de membrana está muy lejos de su valor umbral. La entrada del Cloro ha vuelto más negativo el LIC. Acetilcolina: Tiene receptores de tipo nicotínico y muscarínico.
Es un NT muy frecuente en las sinapsis del Sistema Nervioso Periférico (SNP). Por ejemplo es el NT de las sinapsis: Neuromusculares entre el sistema nervioso motor voluntario y el músculo estriado esquelético. Del Sistema Nervioso Autónomo entre las neuronas pre y post ganglionares simpáticas y parasimpáticos y entras las neuronas postganglionares parasimpáticas y sus efectores. En el SNC es poco frecuente. Se encuentra en el núcleo de Meynert que se haya ubicado en el encéfalo basal anterior. Este núcleo es profundamente estudiado en la actualidad porque son sus neuronas las primeras en deteriorarse en los enfermos con la enfermedad de Alzheimer
La vía de recompensa y motivación, relacionada con TODAS las adicciones conocidas, está tapizada de receptores de nicotina a la acetilcolina. De allí el terrible poder adictivo del cigarrillo. Dopamina: La “reina” del Parkinson, la adicción y la Esquizofrenia. La Dopamina es un NT poco frecuente en el SNC pero de una enorme importancia funcional. Es el neurotransmisor de la vía que conecta a la Sustancia Negra con el Cuerpo Estriado en los Ganglios de la Base. La enfermedad de Parkinson se debe a la muerte de neuronas dopaminérgicas. También es el NT de la vía Meso-Límbica que comunica el Tegmentum Mesencefálico (en el Tronco Cerebral) con el núcleo Accumbens (un Ganglio de la Base relacionado funcionalmente con el Sistema Límbico). Esta vía es activada por TODAS las recompensas naturales (comida, sexo y bebida) y no naturales (alcohol, cigarrillos, cocaína, anfetaminas, LSD, opio, morfina, etc.[7]). Todas las sustancias adictivas aumentan los niveles de Dopamina en esta vía y generan una sensación de placer y excitación psicomotriz. Finalmente la Dopamina conecta el Tegmentum Mesencefálico con la corteza Prefrontal y en los pacientes con Esquizofrenia existiría una elevación anormal de los niveles de Dopamina en la Corteza Prefrontal. Noradrenalina: En el SNP es el NT de las neuronas postganglionares simpáticas sobre sus electores.
En el SNC se encuentra casi exclusivamente en las neuronas de un pequeño núcleo del tronco cerebral denominado Locus Coeruleus. Este núcleo noradrenérgico está relacionado con los niveles de atención. Es el que usted intenta activar cuando toma una taza de café tratando de no quedarse dormido mientras está leyendo estas aburridisimas páginas de neurofisiología. La anfetamina también aumenta los niveles de noradrenalina en este núcleo y lo mantendrá más tiempo despierto. Pero no se lo aconsejo como método “coadyuvante” para aumentar el número de horas de estudio, porque estará tan excitado que no podrá concentrarse para estudia
Serotonina: Este NT sólo se encuentra en el SNC en los núcleos del Rafe ubicados en el Tronco Cerebral. Su disminución está relacionada con ciertos cuadros de depresión “orgánica”*8+. Muchos fármacos antidepresivos (entre ellos el famoso Prozac) actúan bloqueando la recaptación presináptica de la Serotonina para que éste persista en la hendidura sináptica activando a los receptores postsinápticos y aumentar así sus efectos. Endocannabinoides: En general cuando una sustancia actúa sobre nuestro SNC es porque éste ya la tiene. Un ejemplo es la Marihuana (alias Cannabis Sativa). El SNC tiene un tipo de neurotransmisores que se denominan endocannabinoides porque tienen una estructura similar a la Cannabis. Entre sus características particulares está el hecho de que es un NT que va a “contramano”. Con esto quiero decir que se libera desde la postsinapsis hacia la presinapsis, se supone que con funciones de retroalimentación negativa. Los endocannabinoides tienen efectos psicotrópicos[9] ya que producen cambios en la percepción, el estado de ánimo y de conciencia y el comportamiento. También aumentan el apetito, producen analgesia y son antieméticos (inhiben el reflejo del vómito). Por estos efectos existe en la actualidad un debate acerca de su utilización como fármacos para el tratamiento paliativo en pacientes terminales (cáncer y SIDA). Neurotransmisores “no clásicos”: Se han descubierto en la última década algunos tipos de NT que no cumplen con los “dogmas” de la neurotransmisión “clásica”, o sea con el S.A.L.I.D. Describiremos como ejemplo de NT no tradicional al Oxido Nítrico:
· Síntesis: Es un gas tóxico inestable de vida corta.
· Almacenamiento: No se almacena en vesículas.
· Liberación: No depende del Calcio y NO se libera por exocitosis sino que difunde a través de la membrana pre y postsináptica.
· Interacción con receptor: No interactúa con receptores postsinápticos sino que actúa directamente sobre moléculas de segundos mensajeros.
· Desactivación: Se inactiva en forma espontánea y pasiva. Luego de analizar a este NT de una “historia” tan particular ya no queda muy claro cuáles son los criterios para clasificar a una molécula como un NT. ¿No? Es así que el concepto de lo que es un Neurotransmisor, forjado en el siglo XX, seguramente será reevaluado y modificado a la luz del descubrimiento de moléculas que cooperan en la “conversación” entre las neuronas y que tienen características tan disímiles en su síntesis, almacenamiento, liberación, interacción y desactivación.
5.- Desactivación del NT: ¿Por qué debe ser desactivado un NT luego de su interacción con el receptor postsináptico? Hoy a la mañana, ¿qué diario quiso leer el de hoy o el de ayer? El de hoy por supuesto. Lo mismo le pasa a la neurona. Una vez que el NT ha sido liberado por exocitosis ya es “historia vieja” como información del estado funcional de la neurona presináptica. Por eso, una vez que interactuó con receptor postsináptico y le transmitió su información debe ser rápidamente removido para dejar su lugar a una nueva molécula de NT que traiga “noticias frescas” de la presinapsis.
Existen múltiples tipos de desactivación del NT: Desactivación enzimática: Un ejemplo es la Acetilcolina que es destruida por una enzima en la hendidura sináptica. Este tipo de desactivación es el menos “económico” ya que obliga a re-sintetizar al NT. Debemos recordar que es el mecanismo de desactivación de NT más primitivo (el primero que aparece en el árbol filogenético). Difusión al líquido extracelular: Aquí el NT por diferencia de concentración se separa del receptor postsináptico y difunde hacia el líquido extracelular que rodea a la hendidura sináptica. No es un mecanismo muy comúnmente utilizado.
Recaptación:
Recaptación Neuronal: Recaptación Presináptica: El NT es recaptado hacia el terminal presináptico por bombas específicas. La Noradrenalina y la Serotonina son dos ejemplos de este tipo de desactivación que es sumamente “económico” ya que la molécula de NT puede ser rápidamente reutilizada. Recaptación Postsináptica: El NT es recaptado por el terminal postsináptico. Este es un mecanismo infrecuente de desactivación. Recaptación Glial: El NT es recaptado por las células gliales que rodean a la hendidura sináptica. Un ejemplo típico de este tipo de desactivación es el Glutamato.
Principales neurotransmisores Un neurotransmisor (NT) es una sustancia química liberada selectivamente de una terminación nerviosa por la acción de un PA, que interacciona con un receptor específico en una estructura adyacente y que, si se recibe en cantidad suficiente, produce una determinada respuesta fisiológica. Para constituir un NT, una
sustancia química debe estar presente en la terminación nerviosa, ser liberada por un PA y, cuando se une al receptor, producir siempre el mismo efecto. Existen muchas moléculas que actúan como NT y se conocen al menos 18 NT mayores, varios de los cuales actúan de formas ligeramente distintas.
Los aminoácidos glutamato y aspartato son los principales NT excitatorios del SNC. Están presentes en la corteza cerebral, el cerebelo y la ME. El ácido g-aminobutírico (GABA) es el principal NT inhibitorio cerebral. Deriva del ácido glutámico, mediante la decarboxilación realizada por la glutamatodescarboxilasa. Tras la interacción con los receptores específicos, el GABA es recaptado activamente por la terminación y metabolizado.
La glicina tiene una acción similar al GABA pero en las interneuronas de la ME. Probablemente deriva del metabolismo de la serina.
La serotonina (5-hidroxitriptamina) (5-HT) se origina en el núcleo del rafe y las neuronas de la línea media de la protuberancia y el mesencéfalo. Deriva de la hidroxilación del triptófano mediante la acción de la triptófano-hidroxilasa que produce 5-hidroxitriptófano; éste es descarboxilado, dando lugar a la serotonina. Los niveles de 5-HT están regulados por la captación de triptófano y por la acción de la monoaminooxidasa (MAO) intraneuronal. La acetilcolina es el NT fundamental de las neuronas motoras bulbo-espinales, las fibras preganglionares autónomas, las fibras colinérgicas posganglionares (parasimpáticas) y muchos grupos neuronales del SNC (p. ej., ganglios basales y corteza motora).
Se sintetiza a partir de la colina y la acetil-coenzima A mitocondrial, mediante la colinacetiltransferasa. Al ser liberada, la acetilcolina estimula receptores colinérgicos específicos y su interacción finaliza rápidamente por hidrólisis local a colina y acetato mediante la acción de la acetilcolinesterasa. Los niveles de acetilcolina están regulados por la colinacetiltransferasa y el grado de captación de colina.
La dopamina es el NT de algunas fibras nerviosas y periféricas y de muchas neuronas centrales (p.ej., en la sustancia negra, el diencéfalo, el área tegmental ventral y el hipotálamo). El aminoácido tirosina es captado por las neuronas dopaminérgicas y convertido en 3,4-dihidroxifenilalanina (dopa) por medio de la tirosina-hidroxilasa. La dopa se descarboxila hasta dopamina por la acción de la descarboxilasa de l-aminoácidos aromáticos. Tras ser liberada, la dopamina interactúa con los receptores dopaminérgicos y el complejo NT-receptor es captado de forma activa por las neuronas presinápticas. La tirosina-hidroxilasa y la MAO regulan las tasas de dopamina en la terminación nerviosa. La noradrenalina es el NT de la mayor parte de las fibras simpáticas posganglionares y muchas neuronas centrales (p. ej., en el locus ceruleus y el
hipotálamo). El precursor es la tirosina, que se convierte en dopamina, ésta es hidroxilada por la dopamina b-hidroxilasa a noradrenalina. Cuando se libera, ésta interactúa con los receptores adrenérgicos, proceso que finaliza con su recaptación por las neuronas presinápticas, y su degradación por la MAO y por la catecol-O-metiltransferasa (COMT), que se localiza sobre todo a nivel extraneuronal. La tirosina-hidroxilasa y la MAO regulan los niveles intraneuronales de noradrenalina.
La b-endorfina es un polipéptido que activa muchas neuronas (p. ej., en el hipotálamo, amígdala, tálamo y locus ceruleus). El cuerpo neuronal contiene un gran polipéptido denominado proopiomelanocortina, el precursor de varios neuropéptidos (p. ej., a, b y g-endorfinas). Este polipéptido es transportado a lo largo del axón y se divide en fragmentos específicos, uno de los cuales es la bendorfina, que contiene 31 aminoácidos. Tras su liberación e interacción con los receptores opiáceos, se hidroliza por acción de peptidasas en varios péptidos menores y aminoácidos.
La metencefalina y leuencefalina son pequeños péptidos presentes en muchas neuronas centrales (p. ej., en el globo pálido, tálamo, caudado y sustancia gris central). Su precursor es la proencefalina que se sintetiza en el cuerpo neuronal y después se divide en péptidos menores por la acción de peptidasas específicas. Los fragmentos resultantes incluyen dos encefalinas, compuestas por 5 aminoácidos cada una, con una metionina o leucina terminal, respectivamente. Tras su liberación e interacción con receptores peptidérgicos, son hidrolizadas hasta formar péptidos inactivos y aminoácidos, como son las dinorfinas y la sustancia P.
Las dinorfinas son un grupo de 7 péptidos con una secuencia de aminoácidos similar, que coexisten geográficamente con las encefalinas. La sustancia P es otro péptido presente en las neuronas centrales (habénula, sustancia negra, ganglios basales, bulbo e hipotálamo) y en alta concentración en los ganglios de las raíces dorsales. Se libera por la acción de estímulos dolorosos aferentes. Otros NT cuyo papel ha sido establecido menos claramente son la histamina, la vasopresina,la somatostatina, el péptido intestinal vasoactivo, la carnosina, la bradicinina, la colecistocinina, la bombesina, el factor liberador de corticotropina, la neurotensina y, posiblemente, la adenosina.
Principales receptores Los receptores de los NT son complejos proteicos presentes en la membrana celular. Los receptores acoplados a un segundo mensajero suelen ser monoméricos y tienen tres partes: una extracelular donde se produce la glucosilación, una intramembranosa que forma una especie de bolsillo donde se supone que actúa el NT y una parte intracitoplasmática donde se produce la unión de la proteína G o la regulación mediante fosforilación del receptor. Los receptores con canales iónicos son poliméricos. En algunos casos, la activación del recepto
induce una modificación de la permeabilidad del canal. En otros, la activación de un segundo mensajero da lugar a un cambio en la conductancia del canal iónico. Los receptores que son estimulados continuamente por un NT o por fármacos (agonistas) se hacen hiposensibles (infrarregulados); aquellos que no son estimulados por su NT o son bloqueados crónicamente (antagonistas) se hacen hipersensibles (supra regulados). La suprarregulación o infrarregulación de los receptores influye de forma importante en el desarrollo de la tolerancia y dependencia física. La retirada es un fenómeno de rebote debido a una alteración de la afinidad o densidad del receptor. Estos conceptos son particularmente importantes en el trasplante de órganos o tejidos, en los que los receptores están deprivados del NT fisiológico por denervación. La mayoría de NT interactúan principalmente con receptores postsinápticos, pero algunos receptores están localizados a nivel presináptico, lo que permite un control estricto de la liberación del NT.
Los receptores colinérgicos se clasifican en nicotínicos N1 (en la médula adrenal y los ganglios autónomos) o N2 (en el músculo esquelético) y muscarínicos m1 (en el sistema nervioso autónomo, estriado, corteza e hipocampo) o m2 (en el sistema nervioso autónomo, corazón, músculo liso, cerebro posterior y cerebelo).
Los receptores adrenérgicos se clasifican en a1 (postsinápticos en el sistema simpático), A2 (presinápticos en el sistema simpático y postsinápticos en el cerebro), b1(en el corazón) y b2 (en otras estructuras inervadas por el simpático).
Los receptores dopaminérgicos se dividen en D1, D2, D3, D4 y D5. D3 y D4
desempeñan un papel importante en el control mental (limitan los síntomas negativos en los procesos psicóticos) mientras que la activación de los receptores D2 controla el sistema extrapiramidal.
Los receptores de GABA se clasifican en GABAA (activan los canales del cloro) y GABAB (activan la formación del AMP cíclico). El receptor GABAA consta de varios polipéptidos distintos y es el lugar de acción de varios fármacos neuroactivos, incluyendo las benzodiacepinas, los nuevos antiepilépticos (p. ej., lamotrigina), los barbitúricos, la picrotoxina y el muscimol.
Los receptores serotoninérgicos (5-HT) constituyen al menos 15 subtipos, clasificados en 5-HT1 (con cuatro subtipos), 5-HT2 y 5-HT3. Los receptores 5-HT1A, localizados presinápticamente en el núcleo del rafe (inhibiendo la recaptación presináptica de 5-HT) y postsinápticamente en el hipocampo, modulan la adenilato-ciclasa. Los receptores 5-HT2, localizados en la cuarta capa de la corteza cerebral, intervienen en la hidrólisis del fosfoinosítido (v. tabla 166-2). Los receptores 5HT3 se localizan presinápticamente en el núcleo del tracto solitario
Los receptores de glutamato se dividen en receptores ionotropos de N-metil-daspartato (NMDA), que se unen a NMDA, glicina, cinc, Mg++ y fenciclidina (PCP, también conocido como polvo de ángel) y producen la entrada de Na+ , K+ y Ca++; y receptores no-NMDA que se unen al quiscualato y kainato. Los canales no-NMDA son permeables al Na+ y K+ pero no al Ca++. Estos receptores excitadores median en la producción de importantes efectos tóxicos por el incremento de calcio, radicales libres y proteinasas. En las neuronas, la síntesis del óxido nítrico (NO), que regula la NO-sintetasa, aumenta en respuesta al glutamato.
Los receptores opiáceos (de endorfina-encefalina) se dividen en m1 y m2 (que intervienen en la integración sensitivo-motora y la analgesia), D1 y D2 (que afectan a la integración motora, la función cognitiva y la analgesia) y k1, k2 y k3 (que influyen en la regulación del balance hídrico, la analgesia y la alimentación). Los receptores s, actualmente clasificados como no-opiáceos se unen a la PCP y se localizan fundamentalmente en el hipotálamo.
Transporte de los neurotransmisores Existen dos tipos de transportadores de los NT esenciales para la neurotransmisión. El transportador de recaptación, localizado en las neuronas presinápticas y en las células plasmáticas, bombea los NT desde el espacio extracelular hacia el interior de la célula. Repone el abastecimiento de NT, ayuda a concluir su acción y, en el caso del glutamato, mantiene sus niveles por debajo del umbral tóxico. La energía necesaria para este bombeo del NT proviene del ATP. El otro tipo de transportador localizado en la membrana de las vesículas concentra el NT en las mismas para su posterior exocitosis. Estos transportadores son activados por el pH citoplasmático y el gradiente de voltaje a través de la membrana vesicular. Durante la anoxia y la isquemia cambia el gradiente iónico transmembrana, y el glutamato se transporta desde las vesículas hasta el citoplasma, aumentando su concentración hasta niveles potencialmente tóxicos
Los sistemas de segundo mensajero consisten en proteínas G reguladoras y proteínas catalíticas (p. ej., adenilato-ciclasa, fosfolipasa C) que se unen a los receptores y a los efectores. El segundo mensajero puede ser el desencadenante de una reacción en cadena o el blanco de una vía reguladora
UNIÓN NEUROMUSCULAR La unión neuromuscular es básicamente el conjunto de un axón y una fibra muscular. El axón o terminal nerviosa adopta al final, en la zona de contacto con el músculo, una forma ovalada de unas 32 micras de amplitud. En esta zona final del axón se hallan mitocondrias y otros elementos que participan en la formación y almacenaje del neurotransmisor de la estimulación muscular: la acetilcolina. Al otro lado de la terminal axónica se encuentra la membrana celular de la fibra muscular. A esta zona se la denomina placa motora. La zona intermedia entre la terminal nerviosa y la placa motora se denomina hendidura sináptica. La forma de la placa motora es la de una depresión con pliegues y se debe a que debe adaptarse a la forma de la terminal nerviosa y por los pliegues consigue aumentar mucho su superficie.
CONCLUSION
La principal función del sistema nervioso es captar y procesar las señales del organismo para ejercer así control sobre los demás órganos del cuerpo.
Y esto nos permite comprender muchas de las conductas en el ser humano, y en las funciones que desempeñan. Y así comprenderemos la conducta de los organismos ya que generan cambios y podemos ayudar para que interactúe bien con el medio en el que se desarrolla y también socialmente.
Es importante el estudio de las bases biológicos de la psicología porque abarcan en saber cómo es que ocurren los procesos mentales ,donde la unidad importante que propaga el impulso nervioso conociendo cual es la conexión que existe entre el encéfalo y las distintas partes de nuestro cuerpo y sobre todo como es que ocurre esta comunicación en ambas.
Además el saber las causas y porque están fallando y no se propagan adecuadamente y si de alguna manera pueden ser corregir, así que no hay manera de separar la parte psicológica y la conducta biológica en un organismo.
La salud mental es de suma importancia en este conocimiento biológico para el desarrollo de nuevas técnica para tratar condiciones mentales que afectan al ser humano.
También la neuropsicología la cual estudia como la lesión o trauma sobre el sistema nervioso central afecta los procesos psicológico, cognoscitivos y emocionales de un individuo, la psiquiatría que depende directamente del conocimiento que se adquiere en los laboratorios asi como la mayoría de desórdenes psicológicos tienen relación directa con alguna anomalía en neurotransmisiones.
Neurobiología que consta del estudio del sistema nervioso central esta rama trata las neuronas y el transporte de neurotransmisores a través de estas así que esta se conecta con las patologías mentales.
Cada una de ellas tiene una función importante en cada estudio por lo cual se basa en el cerebro y lo cual ayuda a continuar en la búsqueda de adelantos.
Estos avances científicos han permitido que los doctores, y los psicólogos pueden ayudar a las personas con problemas mentales o con psicopatologías, y así mejorar su calidad de vida, con diferentes herramientas.
El psicólogo tiene que tener conocimiento en las bases biológicas para que él pueda ver que es lo que pasa por dentro en el sistema nervioso de su paciente y de donde está surgiendo su síntoma, para que él pueda cambiarlo con el especialista ya sea con el neurólogo o un psiquiatra y el mismo puede combinar diferentes terapias y combinarla con los especialistas.
BIBLIOGRAFÍA:
Neuroanatomía clínica y neurociencia sexta edición.
M j Turlough. Fitzgerald.
M D. PHD. DSC,MRIA.
Gregory Gruener,MD,MBA.
Estomich.MTUI.MD.
Donald B Stratton NEUROFISIOLOGÍA.
Profesor de Biología.Draixe University
Editorial Limusa.
NEUROANATOMIA CLINICA FUNCIONAL
Paul A Young. PH.D.
Profesor and Chairman.dept of
Anatomy and Neurobiología.
St Louis University School Medicine.
Paul H Young.MD.Service Clinical Profesor departamento
De Surgery(neurosurgery)and anatomy and neurobiology
St Louis University School of Medicine.
St Louis Missouri.
García,J.&(2015)Neuroanatomía humana,Madrid:panamericana
John,P(2007) biopsicologia.Madrid,España:pearson educación 6ta edición.
Rosenzweig.M(1997)Psicología Fisiológica.España:Mc Graw

 Al comienzo estábamos circunscritos al estudio de las pérdidas de equilibrio provocadas por el uso de anteojos progresivos, particularmente en el caso de personas mayores. Aclaremos que los anteojos recetados si bien mejoran la imagen percibida por los ojos, siempre introducen una deformación geométrica de la visión, y esta distorsión es mayor hacia la periferia del campo visual. A su vez, el cerebro aprende rápidamente a compensar esa deformación posibilitando con ello la completa adaptación del paciente al uso de sus anteojos. Pero en el caso de los lentes progresivos, concebidos para mejorar el enfoque tanto de objetos lejanos como el de objetos cercanos, se verifica una dificultad mucho más grande de los pacientes para lograr dicha adaptación. Como resultado se percibe una sensación de mareo al girar rápidamente la cabeza. Eso puede generar la ocasional pérdida del equilibrio y provocar caídas, sobretodo en los adultos mayores.
Al comienzo estábamos circunscritos al estudio de las pérdidas de equilibrio provocadas por el uso de anteojos progresivos, particularmente en el caso de personas mayores. Aclaremos que los anteojos recetados si bien mejoran la imagen percibida por los ojos, siempre introducen una deformación geométrica de la visión, y esta distorsión es mayor hacia la periferia del campo visual. A su vez, el cerebro aprende rápidamente a compensar esa deformación posibilitando con ello la completa adaptación del paciente al uso de sus anteojos. Pero en el caso de los lentes progresivos, concebidos para mejorar el enfoque tanto de objetos lejanos como el de objetos cercanos, se verifica una dificultad mucho más grande de los pacientes para lograr dicha adaptación. Como resultado se percibe una sensación de mareo al girar rápidamente la cabeza. Eso puede generar la ocasional pérdida del equilibrio y provocar caídas, sobretodo en los adultos mayores.


